

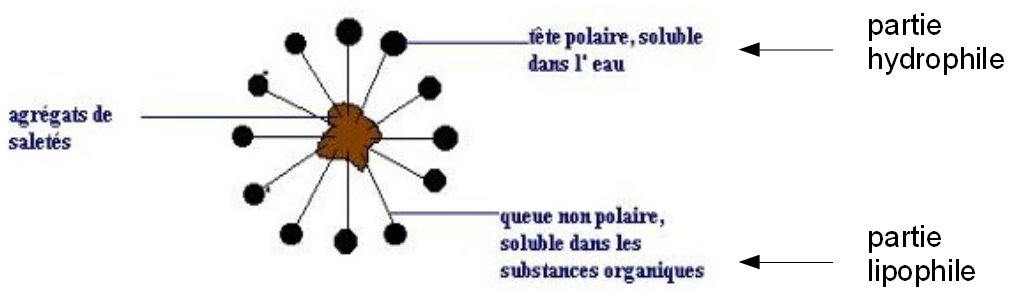

De telles substances sont dites amphiphiles ( du grec amphi "des deux côtés" et philos "ami").
Les frottements permettent aux globules de graisses entourées de tensioactifs de se fractionner et de donner des globules plus petits qui se détachent de l'étoffe et se répartissent dans l'eau de lavage.
TENSION SUPERFICIELLE :
Généralités
Dans un liquide, toutes les molécules sont attirées les unes vers les autres, à cause de forces d' interaction électrostatique, forces de Van der Waals...
Pour les molécules à l'intérieur du liquide, les forces qui s'exercent sur chacune se compensent : |
 |
| Par contre, la résultante des forces qui s'exercent sur les molécules situées à la surface du liquide n'est pas nulle : c'est une force qui attire les molécules vers l'intérieur. |  |
Si par exemple on "casse" une gouttelette d'eau en deux, on va créer de la surface, deux sphères de volume V/2 ont une aire plus grande qu'une seule sphère de volume V. Donc si les deux goutelettes se rencontrent, elles vont avoir tendance à se fusionner pour minimiser la tension superficielle. La tension superficielle est une constante caractéristique d'un liquide.

Capillarité - loi de Jurin :
Un tube capillaire est un tube de petit diamètre intérieur. D'après la loi de Jurin, lorsqu'on plonde un tube capillaire (ouvert aux deux extrémités) dans un liquide, celuis ci "monte" ou "descend" dans le tube dune hauteur h telle que :
 |
avec : r : rayon intérieur du tube p : masse volumique du liquide g : intensité de la pesanteur a : angle de raccordement liquide-solide y : tension superficielle du liquide |
Cette tension pousse la surface de contact entre le liquide et l'air par exemple la plus petite possible, et dans le cas des membranes de savon, cette force pousse la membrane à être la plus petite possible. On peut constater ce phénomène expérimentalement.