

Histoire du savon
Des documents datant de l’Antiquité mentionnent l’usage de nombreuses matières savonneuses et d’agents nettoyants, fabriqués de manière empirique à partir de cendres et de graisses. Dés le 1er siècle ap. J.C, le naturaliste romain Pline l’Ancien décrivait différentes formes de savons durs ou mous et colorés : les rutilandis capillis, dont les femmes se servaient pour se laver les cheveux et leur donner du lustre. Au 8ème siècle, la fabrication industrielle de savons était courante en Italie et en Espagne. Et c’est au 13ème siècle que la France commença à produire industriellement du savon fabriqué à base, essentiellement, de suif de chèvre et de cendres de hêtre (alcali). Vers 1500, les Français mirent au point un savon à base d’huile d’olive en vue de remplacer les graisses animales ce qui était beaucoup moins cher. Cette pratique fut exportée en Angleterre où la production de savon eu beaucoup de succès.
On découvrit ensuite rapidement que le savon peut être produit à partir de graisses extraites de nombreuses espèces vivantes : le suif, la graisse, les huiles de poissons et les huiles végétales, telles que l’huile de coprah (noix de coco), l’huile d’olive, l’huile de palme, l’huile de soja ou l’huile de mais. La fabrication du savon fut révolutionnée en 1791par le chimiste français Nicolas Leblanc, qui mit au point un procédé permettant d’obtenir de la soude caustique à partir du sel de cuisine. Cette soude était capable de réagir avec les graisses pour former du savon beaucoup plus efficace que l’alcali. En 1783, le chimiste suédois Carl Scheele avait fait bouillir de l’huile d’olive avec de l’oxyde de plomb et obtenu une substance au goût sucré qu’il avait appelé Ölsuss et que l’on connaît maintenant sous le nom de glycérine. En 1823, le chimiste français Eugène Chevreul, poussé par cette découverte, découvrit que ce ne sont pas les corps gras qui se combinent avec l’alcali pour former le savon, mais qu’ils sont d’abord décomposés en acides gras et en glycérine (ou glycérol). Chevreul est ainsi à l’origine de la théorie de la saponification.
Au point de vue chimique
Les corps gras sont des triesters du glycérol et d’acides dont le squelette comporte entre 12 et 22 atomes de carbone. Ces esters appelés glycérides sont des constituants des huiles végétales.
Lors d’une hydrolyse basique, c'est-à-dire lors de la réaction d’un ester avec l’eau en milieu basique, les corps gras donnent des ions carboxylates à longue chaîne carbonée. Leur sel de sodium est appelé le savon. L’hydrolyse basique est plus connue sous le nom de saponification dont l’équation de réaction est :
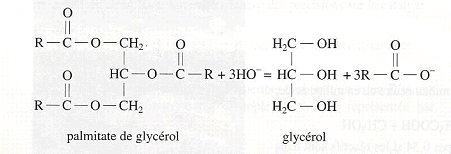
Equation générale de l’hydrolyse basique d’un corps gras. Dans le cas du palmitate de glycérol, R = C15H31.
Lors de la préparation d’un savon, l’hydrolyse basique du corps gras est suivie d’une réaction de précipitation. Pour cela, une solution concentrée de chlorure de sodium est ajoutée à la fin de l’hydrolyse basique. La précipitation qui fournit le savon RCOONa(s) est représentée par l’équation : RCOO_(aq) + Na+(aq) = RCOONa(s)
Cette opération porte le nom de relargage.
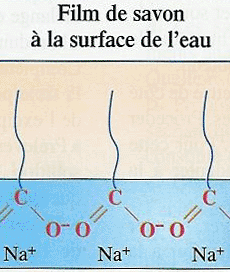
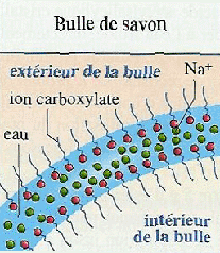
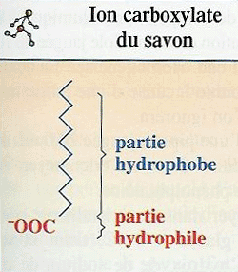
En effet, les ions carboxylates en ayant leur partie hydrophobe en interaction avec les molécules organiques et leur partie hydrophile en interaction avec les molécules d’eau, peuvent empêcher les émulsions de se séparer en une phase grasse (huile) et une phase aqueuse (eau).
Pourquoi le savon lave-t-il ?
Pour enlever une tache, sur un tissu, il faut mettre du savon dans l’eau car l’huile (par exemple) étant hydrophobe, elle ne se mélange pas à l’eau. Si on ajoute du savon dans de l’eau, les queues vont s’accrocher sur la tache (la tête étant tournée vers l’eau). Lorsqu’on frotte, la tache se détache du tissu formant ainsi une micelle. Cette dernière ne colle pas au tissu car sa surface est hydrophile ? Le rinçage emporte le savon et la tache.
Au point de vue chimique…
Les corps gras sont des triesters du glycérol et d’acides dont le squelette comporte entre 12 et 22 atomes de carbone. Ces esters appelés glycérides sont des constituants des huiles végétales.
Lors d’une hydrolyse basique, c'est-à-dire lors de la réaction d’un ester avec l’eau en milieu basique, les corps gras donnent des ions carboxylates à longue chaîne carbonée. Leur sel de sodium est appelé le savon. L’hydrolyse basique est plus connue sous le nom de saponification dont l’équation de réaction est :
Equation générale de l’hydrolyse basique d’un corps gras. Dans le cas du palmitate de glycérol, R = C15H31.
Lors de la préparation d’un savon, l’hydrolyse basique du corps gras est suivie d’une réaction de précipitation. Pour cela, une solution concentrée de chlorure de sodium est ajoutée à la fin de l’hydrolyse basique. La précipitation qui fournit le savon RCOONa(s) est représentée par l’équation : RCOO_(aq) + Na+(aq) = RCOONa(s)
Cette opération porte le nom de relargage.